-
증기의 기본
-
증기의 특성
-
-
-
물의 상태 그래프
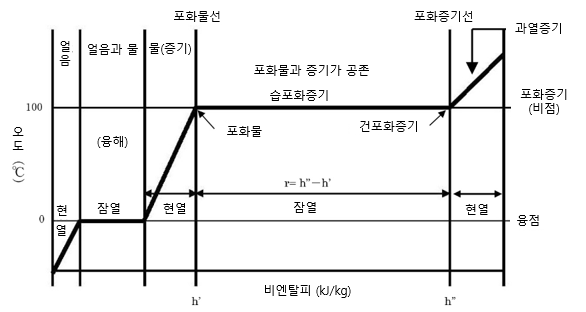
그림 1.1은, 앞선 "물의 상"에서 진술한 내용을 그래프로 나타낸 대기압 하에서 물의 상태를 나타낸 그래프입니다.가로축은 비엔탈피, 세로축은 온도로서 가열(비엔탈피 증가)에 의한 온도와 상변화를 나타냅니다.
(그래프 중앙 좌측 부분의 얼음, 얼음과 물의 혼합상태는 증기 공학분야에서는 그다지 대상으로 하고 있지 않기 때문에 설명은 생략합니다)
-
그림1.1 대기압 하에서 물 상태 변화
온도 0℃에서 가열해서 100℃(비등점)에 도달하기까지 현열(포화수 엔탈피h'), 포화수가모두 증기가 되었을 때의 모든 열량(포화증기의 엔탈피h'), 그리고 그 증발에 필요한 잠열(증발 엔탈피-r=h''-h')이 각각 표시되어 있습니다. 포화수가 증발하는 상태에서 증기는 물과 공존하기 때문에 습포화증기라고 부르며, 모두 증발된 상태의 증기를 건포화증기라고 부릅니다. 건포화증기를 더욱 가열하면 재차 온도가 상승합니다. 이 포화 온도보다도 높은 온도의 증기를 과열증기라고 부르며, 그 과열 증기와 포화 증기의 온도차를 과열도라고 부릅니다.
이 후, 물의 엔탈피를 "현열", 증발 엔탈피를 "잠열", 증기가 보유하는 열을 "전열"로 표기합니다. -
증기 에너지
지금까지 설명에서 알수 있듯이 증기는 가열 등에 사용되어 그 잠열을 잃어버린 후에는
상변화가 일어나 응축수가 되는데, 이 시점의 온도는 증기와 같습니다. 이 특성을 가지는 잠열은
일정 온도에서 안정된 가열 처리를 필요로하는 프로세스와 살균 등에 있어서 상당히 유효한 에너지가 됩니다. 증기가 에너지 운반 수단으로써 뛰어난 이유는 큰 잠열을 보유하면서도 흔한 물질이기 때문입니다.
이 잠열의 크기는 포화 증기표에서 간단히 확인할 수 있습니다. 표1.2는 포화 증기표의 데이터를 일부 발췌한 것입니다. 예를 들면 대기압(게이지압 0.0MPa)에서는 다음 수치가 기재되어 있습니다(소수점 이하는 반올림).・포화수 현열h'=419kJ/kg
・증기 모든열h''=2676kJ/kg
・잠열r=h''-h'=2257kJ/kg
따라서(증기의 모든 열에 대한 잠열 비율) =2,257/2,676=0.8434≒84%
(증기가 보유하는 잠열의 현열에 대한 크기) =2,257/419=5.3866≒5.39
이 같이 대기압 하에서 증기는 그 모든 열 가운데 84%가 잠열이며,
현열의 5.39배나 큰 수치인 것을 알 수 있습니다
표1.1에, 비교적 주변 가까이에 존재하는 물질인 물, 암모니아, 메탄올, 에탄올 열물성을 게재했습니다.
상대적으로 물의 증발열이 현저하게 큰 것을 알 수 있습니다.표1.1 대기압 하에서 주요 물질 열물성
물질
융점(℃)
비점(℃)
융해점 (kJ/kg)
증발열(kJ/kg)
물 0
100
333.5
2,257
암모니아 -77.8
-33.4
338
1,371
메탄올 -97.7
64.7
99.2
1,190
에탄올 -114.1
78.6
109
855
압력이 상승하면, 포화에 이르기 까지 더욱 열량이 필요하며, 온도도 상변화 없이 상승합니다.
바로 현열과 포화온도 양쪽이 증가합니다. 이관계를 표시한 것이 그림 1.2 증기 포화곡선입니다.
이 곡선상에서는 물도 증기도 같은 포화온도로 존재할 수 있습니다. 곡선보다 아래는 아직 포화온도에 도달하지 못한 물이며, 곡선보다 위는 과열 증기입니다.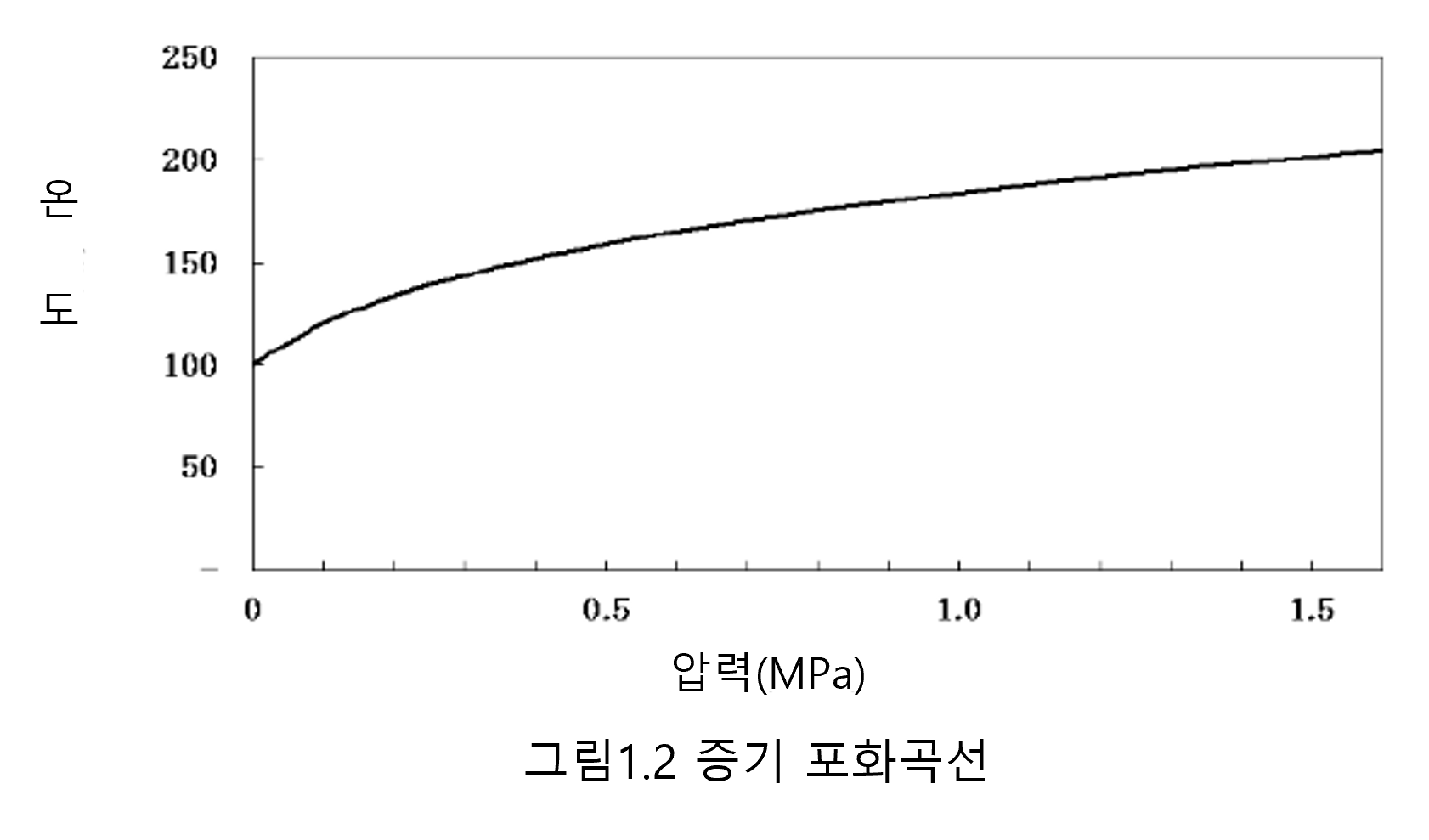
그러면 증기나 포화수 열량은 압력 상승과 함께 어떻게 될까?
그림1.3이 그 관계를 나타내는 그래프입니다. 이 그림에서 다음의 3가지를 알 수 있습니다.①포화수 현열은 압력 상승과 함께 증가합니다.
②증기 잠열은 압력 상승과 함께 감소합니다.
③증기의 모든 열(상기①의 현열과 ②의 잠열의 합)은 압력상승에 대해서 저압역에서는 조금 증가하지만 거의 일정합니다(그러나, 압력 3.2MPa 부근부터는 반대로 감소하고, 임계점에 도달해서는 잠열은 제로가 됩니다)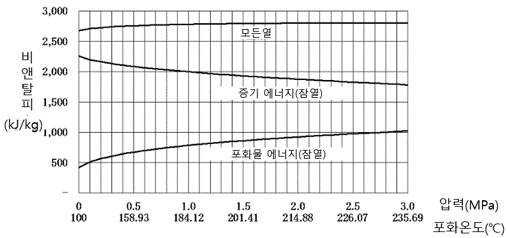
그림1.3 증기 및 포화수 열량과 압력 관계
여기서 주의해야 할 것은 압력 상승에 따라, 증발에 필요한 잠열이 감소하는 것입니다.
이것은 압력이 높은 증기일 수록 이용 가능한 잠열이 적은 것을 의미합니다. 예을 들면 표1.2 포화증기표로부터 압력 증기 0.5MPa과 1.0MPa의 잠열 r은 각각 2085kJ/kg, 1998kJ/kg로 1.0MPa쪽이 작고, 또 모두 대기압 0.0MPa에서 2257kJ/kg보다 작은 수치가 됩니다.
다음으로 증기의 비용적과 압력의 관계를 그림1.4에서 보겠습니다.
그림에서 알 수 있듯이 비용적은 저압역에서는 크게 변화하고, 고압이 됨에 따라 작아지는 반비례적인 변화를 나타냅니다. 압력이 높을 수록 단위 질량(1kg)당 잠열은 감소하지만, 이 용적도 감소하고, 결과적으로 단위용적(1m3)당 잠열을 증가합니다. 따라서 증기 압력을 높임으로써 상대적으로 작은 사이즈의 증기 수송관으로 보다 많은 에너지를 운반하는 것이 가능합니다. 이것은 증기 배관계 설계에 있어서 고려해야할 중요 포인트의 하나입니다.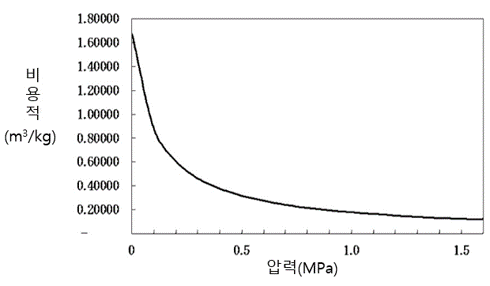
그림1.4 증기 압력과 비용적 관계
표1.2 포화(MPa)
게이지압력(MPa) 포화온도(℃)
비용적(m3/kg) (kg/m3)
비중량 증발열(kJ/kg)
포화수
포화증기
현열
전열
잠열
v’
v”
h’
h”
r=h”-h’
0.0
100.00
0.0010437
1.67300
0.5977
419.06
2676.0
2256.9
0.1
120.44
0.0010610
0.87999
1.1364
505.58
2706.6
2201.0
0.5
158.93
0.0011096
0.31482
3.1764
670.79
2755.6
2084.7
1.0
184.12
0.0011331
0.17718
5.6440
781.36
2779.7
1998.3
-
건도
증기는 보일러에서 생성되어 각 사용장소에 수송되지만, 보일러에서 수분을 전혀 포함하지 않는 증기를 생성하는 것은우선 불가능에 가까우며, 불가피하게 다소의 수분을 포함하게 됩니다. 그러나 증기 사용 측에서 보면 수분을 전혀 포함하지 않는 건포화증기가 바람직합니다. 이 수분 함유량 정도를 건도(Dryness Fraction)라고 하며, 건도가 높을 수록 증기 질(Quality)가 좋다고 할 수 있습니다.
건도(X)는 증기의 중량에 대한 건증기의 중량 비율입니다. 예를 들면, 증기가 5% 수분을 포함하는 건도는
0.95입니다. 덧붙여(1-X)를 습도라고 합니다. 보일러 출구 증기 건도는 대략 0.95~0.98입니다. 습포화증기가 가지는 열량(비엔탈피h)는 그림1.1 기호를 이용하면 다음 식으로 나타낼 수 있습니다.
h=(1-χ)h’+χh”=h’+χr -
플래시 증기
플래시 증기(Flash stem)는 일반적으로 응축수 리시버의 벤트나 스팀 트랩 2차측 개방 응축수 배관에서 생성되는 증기를 표현하기 위해 사용됩니다. 열을 가하지 않는데 어떻게 증기가 생성되는 것인가? 플래시 증기는 어떤 압력의 물이 그것보다 낮은 압력에 노출될 때 그 물 온도가 그 낮은 압력의 포화온도 보다 높을 경우 반드시 발생합니다.
예로서 응축수 스팀 트랩을 통과하는 경우를 생각하면, 1차측 온도는 플래시 증기를 발생시키기에 충분히 높은 온도가 대부분입니다.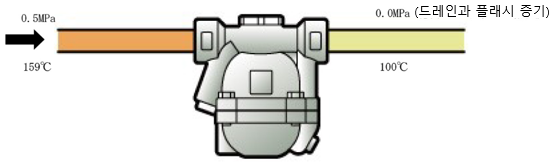
그림1.5 플래시 증기의 생성
그림1.5에서 스팀 트랩 1차측 압력이 0.5MPa로, 그 포화 온도 159℃의 응축수1kg이 대기개방(0.0MPa) 응축수배관으로 배출됩니다.
표1.2에서 0.5MPa 포화온도의 응축수 1kg이 보유하는 현열은 671kJ입니다. 열역학 제1법칙에 의해 유체 전열량은 스팀 트랩의 고압측과 저압측에서 동등하며, 이것은 일반적으로 에너지 보존칙에 따른 것입니다(스팀트랩내에서 방열이나 유로 저항에 의한 열손실은 무시합니다) . 따라서 저압측으로 흘러간 물 1kg도 671kJ 열을 보유하게 됩니다. 그러나 압력 0.0MPa하에서 물은 419kJ 열밖에 보유하지 못하고 671-419=252kJ 열의 불균형이 발생합니다. 이것은 물의 측면에서 보면 잉여 열이 되지만, 이 잉여된 열이 드레인의 일부를 비등시키는, 이른바 플래시 증기를 생성시킵니다.
따라서 트랩의 고압측에서는 액체로서 존재하는 응축수1kg은 저압측에서는 액체와 일부 증기의 형태로 존재하게 됩니다.
생성되는 플래시 증기량은 다음식으로 계산 가능합니다.
따라서 응축수1kg당 플래시 증기 생성량은 0.11kg이 됩니다.
플래시 증기 생성 비율은 그 최종 압력에 있어서 잉여 열과 잠열의 비율으로 생각할 수 있습니다.
중요한 것은 플래시 증기는 단순히 증기 시스템이나 출구에서 자연 발생적으로 생성되는 현상으로간주하는 것이 아니라 증기의 유효 활용을 위해 적극적으로 이용해야 한다는 것입니다.
플래시 증기를 이용하기 위한 대표적인 기기로서는 플래시 탱크가 있습니다. -
기타 특성
증기가 에너지 운반 수단으로 널리 이용되는 이유로서 보유 잠열이 크다는 점, 물이 지구상에 많이 존재해서 경제적인 점 등은 이미 설명한 바와 같지만, 그 밖에 다음의 이유를 들 수 있습니다.
- ・인체에 무해
・부식성이 적고 인화 위험성이 없어서 화학적으로 안정적
・다른 가열 매체에 비해, 균일한 가열을 실행
・압력을 변화에 따라 온도 변화가 일어나지 않아 요구 온도에 따라 공급이 가능
・증기와 드레인의 비용적 차가 크기 때문에 증기가 응축하면 바로 새로운 증기가 공급
-
증기 사용의 과제 사항
・보일러에서 증기 생성 과정이나 그 후 프로세스에서 공기 등의 혼입을 완전히 방지할 수 없어
혼입 공기에 따라 전열 효율이 저하
・증기를 생성하는 원수는 순수한 물이 아니기 때문에 산화 부식 원인이 되는 불순물이 녹아서 존재,
증기 생성 과정에서 그러한 것을 완전 제거가 불가
스팀 트랩에 있어서 물 응고점이 0℃이기 때문에 지역에 따라 동결 방지 대책이 필요합니다.